衛福部食藥署今天(2日)宣布已有26.5萬劑高端疫苗完成封緘檢驗,外界關注高端何時開打。對此,中央流行疫情指揮中心指揮官陳時中表示,20萬劑數量太小、難以排定分配,等到通過檢驗的劑量達到50、60萬劑,就可開始供民眾施打。
高端已於7月18日取得緊急使用授權(EUA),食藥署2日上午宣布,首4批26.5萬劑高端疫苗已完成封緘檢驗,預計傍晚就可放行。
中央流行疫情指揮中心指揮官陳時中2日下午在記者會中表示,高端已送多批疫苗到食藥署檢驗,其中許多批的技術性資料不完整,需要補件再驗,他無法掌握之後能有多少劑量,但現有的20幾萬數量太少、難以分配,至少要有50、60萬劑才會開放民眾預約接種。他說:『(原音)所以你要問我說大概會多少開始,我想大概50、60萬我們就會開始了啦,如果你說20幾萬來開始,那真的很難分,大家施打上,那時間上,如果在50、60萬,大概還有一定量可以來做一個分配,那時候我們就會開始來做。』
陳時中指出,高端疫苗是新的疫苗,與國外已製造幾億劑的疫苗不同,製程還未達到一定的穩定度,雖然供貨相對穩定,但查驗變數較大,因此相關補件、檢驗都比較多,但食藥署進行檢驗封緘絕不含糊。
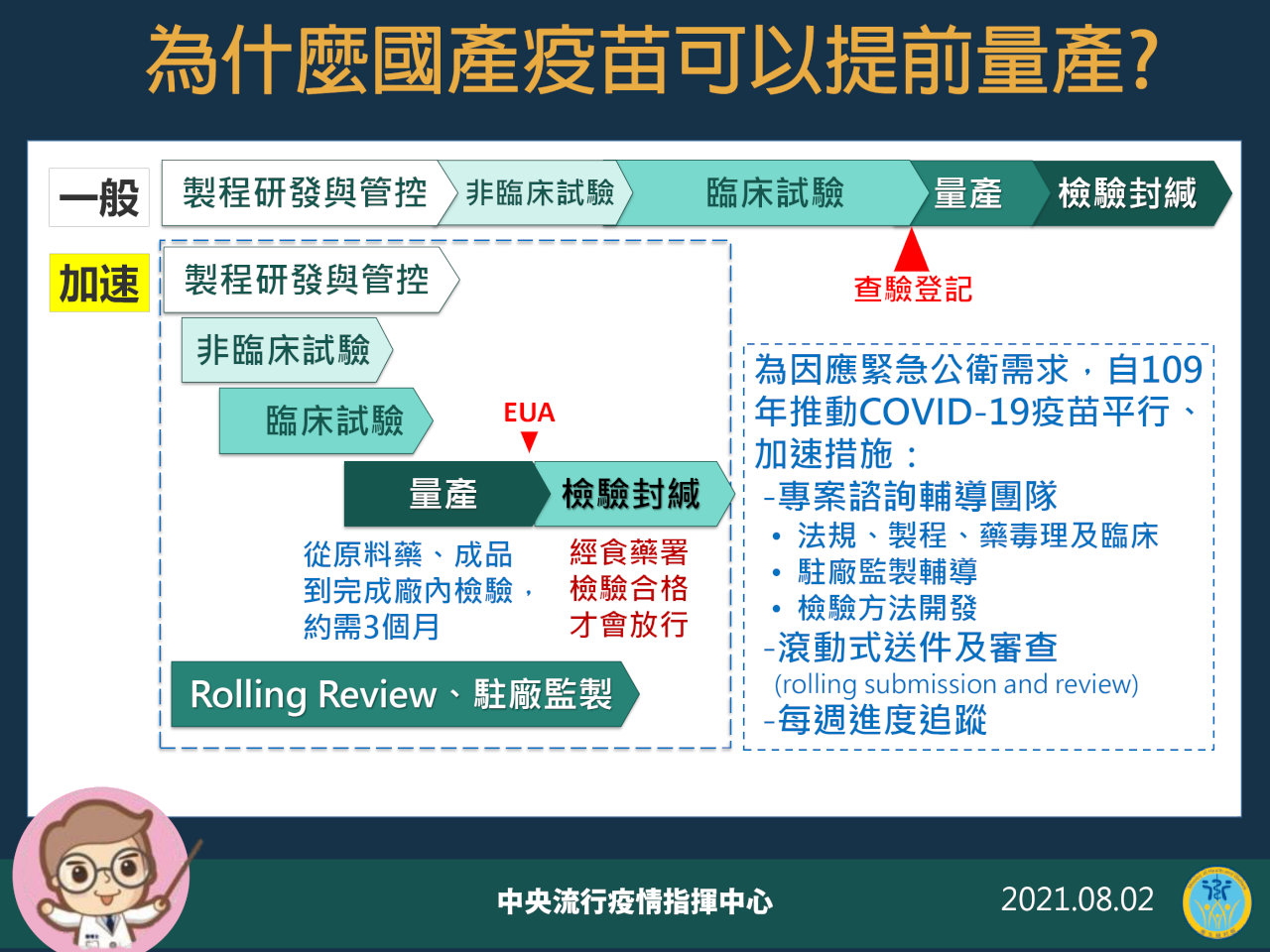
由於高端在取得EUA前便先量產送驗,引發質疑,陳時中也特別詳細說明,這是為因應緊急公衛需求,推動疫苗平行加速措施,如果等EUA通過才開始量產,會拖3、4個月,甚至半年不等,將失去EUA的效益,因此當初跟國產疫苗預採購時,就已談好臨床試驗進行到一定程度時同步量產,若之後EUA未過,政府會負擔前期的研發費用,共同承擔風險,因此廠商才願意先量產。陳時中強調,如果EUA沒過,這些量產的疫苗也無法上市;就算取得EUA,如果封緘檢驗不通過也沒用,一定要每步都合格才會提供民眾使用。
陳時中也透露,另一家國產聯亞疫苗申請EUA,目前還在補件階段,但也已做好19批疫苗送食藥署檢驗。
指揮中心向高端、聯亞各採購500萬劑疫苗,且各有500萬劑的開口合約,媒體詢問什麼條件下會向高端加購500萬劑?陳時中說,以每人打兩劑計算,如果確定只願意打高端的民眾超過250萬人,就會準備加購。
 用Podcast訂閱本節目
用Podcast訂閱本節目  Rti 中央廣播電臺
Rti 中央廣播電臺