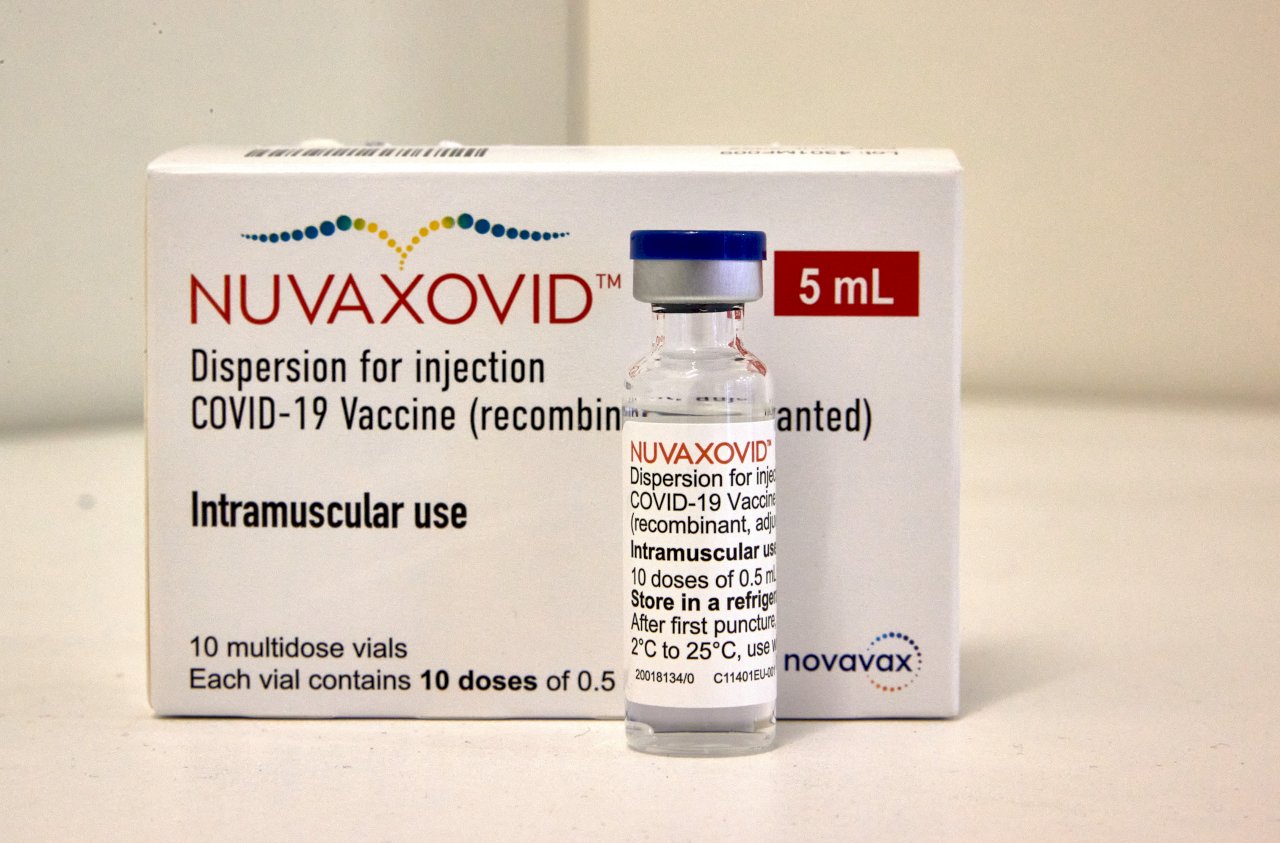
就在專家考慮諾瓦瓦克斯(Novavax)的COVID-19(2019年冠狀病毒疾病)疫苗在美國使用之際,美國食品暨藥物管理局(FDA)3日對這款疫苗和心肌炎的可能關係表達關切。
諾瓦瓦克斯疫苗已在其他國家取得授權,特別是在歐洲。而在美國,一個應FDA要求而召集的獨立委員會將在7日開會,評估諾瓦瓦克斯的臨床實驗數據、並提出建議。
在這之前,FDA在3日公佈一份冗長的文件分析這些結果,就如同對其他3款已獲得美國授權的疫苗所做的那樣。不久後,諾瓦瓦克斯的股價在紐約證交所下跌20%。
根據FDA,在Omicron變異株出現前所進行的試驗中,諾瓦瓦克斯疫苗被發現在對抗這種疾病的有症狀病例具有90%效力。
但在接種疫苗組被發現有6起心肌炎病例,而在安慰組中則發現1例。
據指出,有5例是發生在接種疫苗2週內。
FDA表示,在4萬名臨床試驗參與者中確認了數起可能與疫苗有關的案例,「引發如果有因果關係的話,接種諾瓦瓦克斯疫苗後的心肌炎風險,可能高於像是輝瑞(Pfizer)或莫德納(Moderna)等其他疫苗所通報案例的關切」。
施打輝瑞或莫德納這種信使核糖核酸(messenger RNA,mRNA)疫苗,確實有心肌炎的小風險,特別是在年輕男性和青春期男孩。
但FDA提到在這些疫苗的臨床試驗中並未發現任何病例,而FDA似乎關切諾瓦瓦克斯的風險較高。
諾瓦瓦克斯在3日針對FDA的報告發表聲明說,他們認為並沒有足夠證據來建立起因果關係,而且在任何足夠大型的數據庫中,看到心肌炎的自然基準事件是正常的。
 用Podcast訂閱本節目
用Podcast訂閱本節目