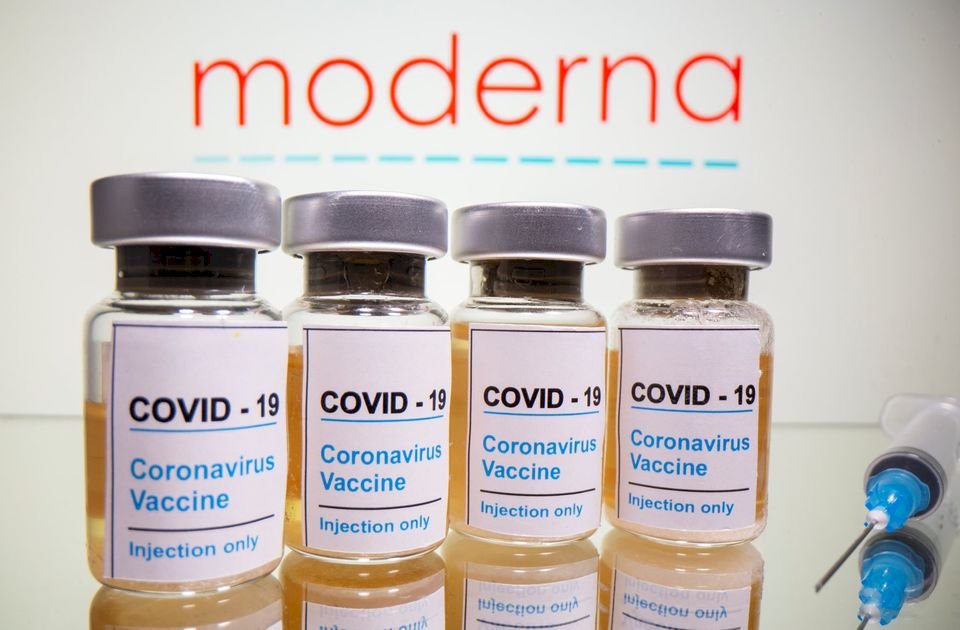
美國食品暨藥物管理局(FDA)18日通過美國藥廠莫德納生技公司(Moderna Inc)疫苗的緊急使用授權(EUA)。這是繼FDA在11日通過美國輝瑞藥廠(Pfizer)與德國生技BioNTech共同研發的COVID-19疫苗緊急使用授權之後,所授權的第二款疫苗。
美國的2019年冠狀病毒疾病(COVID-19)疫情沒有緩和的跡象,目前每天造成超過2,500人死亡。
美國是第一個授權使用莫德納兩劑式疫苗的國家。
FDA局長哈恩(Stephen Hahn)表示,現在美國有兩款預防COVID-19的疫苗可用,FDA已在全球對抗COVID-19方面採取了另一項關鍵步驟。
美國總統川普(Donald Trump)在推特上寫道,「恭喜!莫德納疫苗現在已經獲得授權。」
預定明年1月20日宣誓就職的美國總統當選人拜登(Joe Biden)也對這項消息表達歡迎,並譽為對抗COVID-19的另一項里程碑。
然而,拜登也警告說,未來還有重大挑戰,包括疫苗的製造、分配,以及對數億美國人民接種的艱鉅任務。
英國在12月2日批准對輝瑞與BioNTech疫苗的緊急授權,成為全球第一個授權使用此種疫苗的國家,並在8日率先對英國人民接種,包括美國在內的其他國家則陸續跟進。
截至目前,COVID-19已在美國造成超過31萬3,500人死亡,確診病例逼近1,746萬。
莫德納指出,該公司今年將釋出大約2,000萬劑疫苗給美國政府,預期明年第一季生產1億到1.25億劑疫苗,其中8,500萬劑至1億劑將供給美國。
為了鼓勵美國民眾接種疫苗,美國副總統彭斯(Mike Pence)及其夫人18日在白宮旁的一棟大樓內,經由電視直播,一起公開接種輝瑞與BioNTech疫苗。
延伸閱讀
 用Podcast訂閱本節目
用Podcast訂閱本節目